硬质气管镜(硬镜) 硬镜可作为介入通道,允许各种器械进入气道内,在直视下进行止血、支架释放、取异物、消融治疗(激光、电热和冷冻等)、球囊扩张等操作,与可弯曲支气管镜配合使用可治疗复杂气道疾病。在进行介入操作时,硬镜能同时保证气道通畅和提供呼吸支持,故亦被称为“通气气管镜”。全麻下硬镜操作是诊断儿童气道疾病的主要方法。
一、支气管镜问世前期
早在公元前5世纪,希波克拉底曾尝试给窒息患者经喉插入导管以改善患者的通气。至公元1000年左右,人们开始采用银制导管用于改善窒息患者的通气。18世纪中叶,人们提出了经鼻气管插管治疗呼吸困难及气道异物。此后的几十年间,人们设计了多种器械,并用其通过喉盲取异物获得成功,而此时其他机体腔道器官,如口、鼻、耳、直肠、阴道、膀胱等的检查器械已在临床广泛使用。1853年,Desormeaux首次将其设计的人体腔检查器械称为“内镜(endoscope)”。当时大多采用日光或烛光来满足内镜检查的照明。由于气道检查对照明的要求较高,以至于有人把当时的情形描述为“当时也许只有咽喉及气道的疾病还隐藏在黑暗中,人们难以直接窥视”。
1886年,维也纳的内镜制造商Leiter造出了世界上第一台被称作“通用电内窥镜(panelectroscopy)”检查用器械,它是由管道和手柄两部分组成,为检查提供照明用的电灯泡和反光镜被置于手柄中,此后又有很多这方面的专家对其进行了不断的改进。1894年,德国的Kirstein医生有意识地采用食管镜对喉部进行检查时,偶然地将内镜插入了气管,由此他开始系统地对气管进行直接窥视研究。经过研究后他确信,只要采用可卡因对气管进行充分麻醉后,应用中等尺寸的食管镜完全可以通过声带到达气管分叉处。但同时他也意识到,气管下端是一个十分危险的区域,在插入坚硬的器械时需要严密的监护。
他的这一研究成果在1895年6月4日举行的第二届德国南部喉科医师大会上进行了专题报道。被后人称为“支气管镜之父”的德国佛赖堡大学医院的Gustav Killian医生,在聆听了Kirstein的报告别后立即意识到,Kirstein的观察对于喉和气管疾病的诊断和治疗具有非常重要的意义。从此,Killian与他的同事们采用新的方法开辟了支气管镜使用的新纪元。
二、Gustav Killian与硬质支气管镜的发明
Gustav Killian(右图)1860年6月2日出生于德国Mainz。1878年中学毕业以后即进入斯特拉斯堡大学学习医学。1880年以后,他先后在佛赖堡、柏林和海德堡等地接受临床教育,1882年毕业后在海德堡附近的曼海姆的一所医院从事临床工作,后又到柏林进修耳鼻喉科。1887年,他受聘担任了佛赖堡一所内科医院的鼻喉科主任。
在十九世纪末,随着电光源的发明,采用可卡因对气管进行局部麻醉方法的成熟以及各种内镜器械的不断完善,为支气管镜的问世奠定了基础。1895年在听了Kirstein医生所介绍的新技术以及 Pieniazek 报道的采用检查器械通过气管造口处进入并对气管进行直接观察的经验后,Killian很快意识到这种直接观察气管的新方法具有的重要意义,并于1896年开始了支气管镜的试验工作。
Killian首先采用经过改良的食管镜,对气管切开患者的气管进行观察,并越过窿突对两侧的支气管进行逐叶观察。后经过无数次在未行气管切开的尸体上进行练习,1897年,Killian首次在一名志愿者身上进行试验,他将内镜通过喉直接对气道进行观察,并且发现气管具有一定的弹性,调整好角度后内镜很容易进入两侧的主支气管,并能看到叶支气管水平。Killian非常兴奋,并记下了当时的情形,“我想我有了一个重大发现”-―支气管镜从此诞生了。同年,Killian应用这一硬质支气管镜经喉为一例气管异物的患者进行了异物摘除术,这在当时是一项非常了不起的创举。因为在当时胸外科还不能进行肺叶切除手术,因此大多数异物吸入后的患者都将经历肺不张、反复的肺部感染和咯血等,若不治疗将有近半数的患者死亡。在此之后他们又成功地从2例患者的气道内将异物取出。
经过不断地完善以后,Killian将他的直视支气管镜新方法在1898年5月召开的第6届德国南部喉科医师协会的年会上作了报道,同年他的第一部有关直视支气管镜的出版物也与读者见面。在以后的几年里,为了满足适应证不断扩大的需求,硬质支气管镜技术被进一步完善。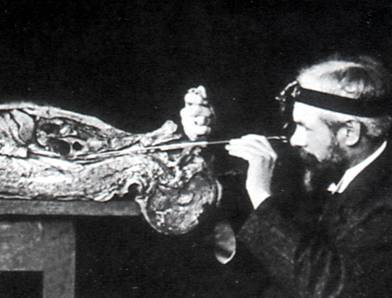
Killian本人也相继发表了34篇有关支气管镜的发明、技术改进及临床应用等方面的文章。1900年,Killian因其“支气管镜及其在肺部异物中的应用”一文而获得殊荣,弗赖堡也变成了支气管镜的圣地。每年有来自世界各地的数百名医生前往弗赖堡参观学习,开设的训练班也多达20期。与此同时,Killian也经常被邀请到欧洲各国作巡回演讲,世界各地的气道异物患者也纷纷慕名前去接受治疗。据统计,在1911年至1921年的10年间,Killian共为703例气道异物患者进行了手术,除 12例患者手术失败外,其余的患者全部治愈,手术的成功率为98.3%。
Killian一生除了发明支气管镜,并将其成功地用于气道异物摘除外,还有多项技术发明,如采用支气管镜对肺脓肿患者进行脓液引流和脓腔内注药;将支气管镜用作胸腔镜对脓胸实施引流;采用金属扩张器对异物刺激而引起的肉芽增生进行扩张;对异物摘除后气道仍有狭窄者,采用金属和橡胶作为支架植入到狭窄处等。1914年,他们还采用新钍(mesothorium)对喉癌患者实施腔内放射治疗,这也是自有腔内近距离放射治疗以后,成功治愈气道内肿瘤的首例报道。这些理念和技术至今仍被临床沿用。以致于后人这样评论他:“Killian点燃了同时代人将技术推广至其他专业的热情,他的杰出贡献为当代气管内麻醉和气道腔内介入治疗奠定了基础。
三、硬质支气管镜的临床应用现状
(一)现代硬质支气管镜的演变 继 Killian之后,人们不断地对硬质支气管镜进行改进,较具代表性的人物是美国的Chevalier Jackson医生,1904年他制造了美国的第一台支气管镜,此后他又在其支气管镜的远端装上了一个小灯泡,同时还增加了一个吸引通道,此外他还设计出了一系列用于取异物的辅助器械。1907年,他出版了第一部系统介绍气管食管病学的教科书,在书中他详细阐述了支气管镜室的设计、设施和人员安排;支气管镜检查的操作规范;并发症的预防及处理等问题。Jackson医生因此而被喻为:“美国的气管食管病学之父”(下图)。可以说正是由于Killian和 Jackson两人的努力,为现代硬质支气管镜的发展奠定了坚实的基础。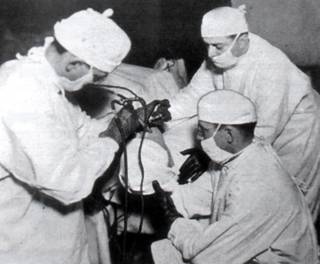
1962年,日本学者Shigeto Ikeda,也就是后来纤维支气管镜的发明人,将玻璃纤维导光照明方法引入到硬质支气管镜中。1963年,Storz K首次采用Hopkins的杆状透镜和纤维导光技术制成冷光源并应用于他发明的硬质支气管镜中,基本形成了现代硬质支气管镜的雏形。
现代硬质支气管镜分别由镜体和杆状透镜组成,外套管是由一根直径相同的直的空心金属管,管腔的形状接近于园形,管壁厚2~3 mm,成人硬质支气管镜的直径范围为9~13.5 mm,镜体长约40 cm。镜子的远端是一个斜面,这样更容易通过声门和狭窄区。同时斜面的边缘也可以用作切除气道壁上的肿瘤。另外,在镜筒的前1/3部分分别有用于通气的孔道,这样即使是镜体伸到了一侧支气管,这些通气孔仍能保证对侧肺的通气。在其操作端分别含有电镜入口、通气孔、吸引孔和活检孔
(二)硬质支气管镜的临床适应证和禁忌证 从 20世纪初开始,硬质支气管镜作为气道病变诊断与治疗的惟一的手段,一直延用了将近70年。只是在20世纪70年代以后,纤维支气管镜以其所具有的多项优点,很快在气道病变的诊断和治疗方面占尽了优势。尽管如此,硬质支气管镜仍在某些领域发挥着重要作用,特别是支气管腔内介入治疗的兴起,硬质支气管镜又重新引起了广大肺内科、胸外科以及肿瘤科医生的兴趣。
1.适应证
(1)诊断方面:①气道深层组织的活检。②儿童的支气管镜检查。③获取更好的图像资料。
(2)治疗方面:①大咯血的治疗。②气道狭窄的扩张。③气道腔内的激光治疗。④气道腔内支架植入。⑤气道的异物摘除。⑥气道腔内的肿瘤切除。⑦冷冻治疗。⑦电凝治疗。
2.禁忌证 ①血流动力学指标不稳定者。②顽固性的低氧血症。③因脊椎关节强直造成脊椎活动受限者。④颌面部外伤或口腔疾病造成张口受限者。⑤喉部疾病(如肿瘤等)造成硬质镜通过困难者。对于此类患者可行气管切开术后,经气管套管进行硬质镜检查。
(三)展望 随着纤维支气管镜的普及,特别是20世纪80~90年代硬质支气管镜的临床使用频率急骤下降,以至于很多医院的硬质支气管镜长期闲置。根据1990年在对美国1 000名肺科医师的调查发现,96%的肺科医师仅使用纤维支气管镜,能够操作硬质支气管镜的只有8%;1 700名胸外科医师中,能够熟练操作硬质支气管镜者也仅为8.4%。多数医师对硬质支气管镜缺乏经验,未接受过良好的培训。我国的情况大致相仿,根据我们近期的一项调查显示,呼吸内科医师掌握硬质支气管镜操作技术者,不到3%。究其原因主要是因为:①硬质镜的操作,大多要在全麻下进行,患者不易接受。②硬质镜的可视范围有限。③操作人员需要经过专门的特殊训练。
但自1990年以后,随着激光、电凝、冷冻、球囊扩张以及支架植入等各种气道腔内介入治疗的广泛开展,硬质支气管镜又重新受到人们的重视。由于硬质支气管镜所具有的定位准确、操作过程可在机械通气的支持下进行,并可对阻塞的气道直接进行扩张和新生物切割等特点,从而明显提高了气管、支气管腔内介入治疗的安全性。相信随着各种气道腔内介入治疗的进一步开展,硬质支气管镜将会继续在呼吸病的诊治中发挥重要作用。
现代硬质支气管镜系统主要有镜体、杆状透镜及光源三部分组成。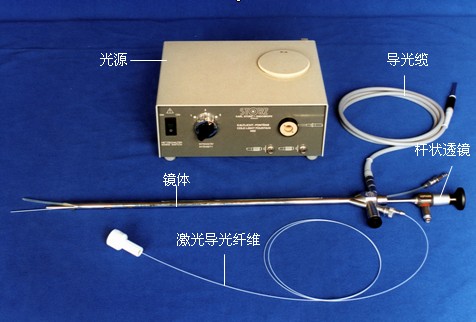
一、镜体
现代硬质支气管镜的镜体为一空心不锈钢管,远近端直径均一。成人硬质支气管镜的直径在9~13.5 mm;长度一般为40 cm;管壁的厚度在2~3 mm。镜体的远端的斜面,这一结构特点有助于通过声门和气道的狭窄部分,同时还可以用其铲除阻塞于腔内病灶。在远端1/3的镜体上有侧孔,便于镜体深入一侧气道时,而不影响对侧气道的通气。
在镜体的近端通常有一个中央开口和几个侧孔组成。操作时所用的硬质杆状透镜,各种活检镜、异物钳、吸引导管、穿刺镜、扩张用的球囊、探条、激光导光纤维、支架的推送装置等均可通过中央开口送入。近端的侧孔可用于连接通气管道和外置光源。
二、杆状透镜
硬质支气管镜的目镜是由一可以提供一定视野和略带放大作用的一组(包括0º、30º、60º、90º和110º)杆状透镜所组成。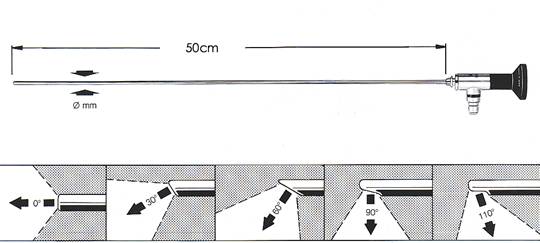

对于大多数的气管及支气管腔内的操作,视角为 0º的杆状透镜都能胜任,而有一定视角的杆状透镜则可清楚地显示两侧的上叶支气管。操作者可根据不同的目的,选择不同的目镜。在杆状透镜的近端可以接上摄像头(图),这样就可将镜下所见及整个操作过程显示在监示器上,同时还可进行录像,或储存在电脑中。
四、其他附件
包括各种类型的活检钳及异物钳。
硬质支气管镜专用的各种活检钳及异物钳
此外还有像扩张用的机械探条、球囊、冷冻探头、电凝头、激光导光纤维、吸引管等。
在临床上,可弯曲支气管镜在操作过程中,由于需要占据一定的气道空间,故可能影响患者的通气功能,这对于健康的成年人一般不会引起通气功能障碍。但对于气道狭窄患者或儿童患者,则可能影响其通气功能,甚至威胁生命安全。由于硬质支气管镜可保留开放的气道空间,并可接高频喷射通气机或呼吸机,故硬质支气管镜又有“通气支气管镜”之称。
一、术前准备
一般硬质支气管镜的操作标准麻醉方式是全身麻醉,因此,应术前进行评估,包括血常规、心电图、血氧饱和度和血气分析、胸部X线及胸部CT检查。此外还需解释有关全身麻醉的程序,解释术后可能会存在一段短时间,甚至数天喉部和口部的不适感。对于头颈不能后仰和上下颌张开困难者,应列为硬质支气管镜检查禁忌症。
二、麻醉方法
一般应用硬质支气管镜需在全身麻醉条件下进行,有时应用非全身麻醉的静脉镇静药亦可达到安全、患者无不适感的目的。对于呼吸衰竭者,硬质支气管镜与呼吸机连接可在保证呼吸道的通畅和供氧的情况下,进行气道的介入性诊断和治疗。
三、患者的体位
患者一般采取仰卧位。全身麻醉后,应采用眼罩和牙垫对眼及牙齿进行保护;采用无菌治疗巾折叠后,将患者头的上半部分盖住。一些医生喜欢将患者的头悬于手术床缘,并将其枕在操作者的大腿上;或由助手用双手将患者的头部托住。这样可使气管被拉向前位,便于支气管镜进入。
四、硬质支气管镜的插入方法
1.直接进入法 传统的硬质支气管镜插入技术,无需借助任何其他辅助设备。硬质支气管镜镜体先用石蜡油润滑,操作者右手持镜的近端,左手拇指和示指分别放于口的上下牙齿之间以保护牙齿和打开上下颚,镜体末端的斜面面向患者的头部,镜体垂直进入口腔,见到悬雍垂后,右手下压硬质支气管镜的近端,镜体远端使舌根部缓慢抬高,这时可暴露会厌,用硬质支气管镜的斜面挑起会厌后可见声门开口,将镜体旋转90º并缓慢推过声门,进入气管后,将镜体回旋90º使斜面保持原位,应用左手指用旋转推进的方式,将支气管镜推进到远端气道(图1-26-1)。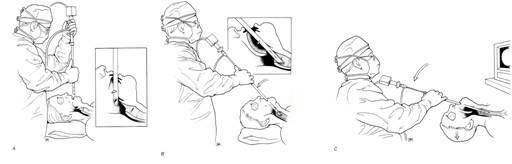
a b c
硬质支气管镜直接进入法示意图
该方法要求操作者要有相当的经验,而对于初学者来说,直接采用此方法可能有一定困难。
2.利用喉镜引导法 按照常规气管插管的操作方式,左手持喉镜使会厌暴露,右手持硬质支气管镜进入喉咽,当硬质支气管镜斜面尖端将要触及会厌时,操作者需要通过硬质支气管镜目镜观察,用硬质支气管镜尖端提起会厌,然后退出喉镜,持镜者将硬质支气管镜顺时针旋转90º,并将硬质支气管镜近端从口腔右侧位移直正中位,直视下将硬质支气管镜缓慢推入气管内(图1-26-2)。进入气管后,将镜体回旋90º使斜面保持原位,旋转将镜体向远端气道推进。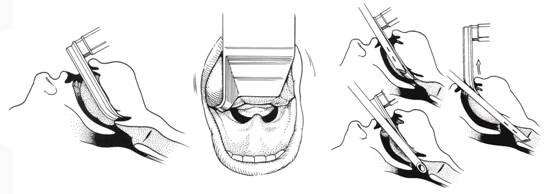
a b c
喉镜引导法示意图
a:;b:显示采用喉镜暴露会厌; c:显示硬质支气管镜沿喉镜方向进入气管
3.利用气管插管方法 先插入气管插管接机械通气并提供适当浓度氧气,将气管插管近端移向口角左侧,将口腔及咽喉分泌物吸引干净。操作者左手打开患者口腔,右手持镜,镜斜面向下,插入患者口腔后部,通过硬质支气管镜目镜观察,当接近舌时,缓慢向前推动镜体,直到声门暴露能够观察到右侧声带和左侧声带前部,然后由麻醉师将气管插管球囊的气体抽空,球囊放松后,见气泡从声门逸出,麻醉师缓慢将气管插管退出,等到气管插管的松驰球囊退到声门外时,操作者将硬质支气管镜顺时针旋转90º,并将镜体近端从口腔右侧位移至正中位,直视下将硬质支气管镜缓慢推入气管内,硬质支气管镜斜面进入气管后,将镜体逆时针旋转90º恢复镜体斜面方向(图 1-26-3)。麻醉师将气管插管缓慢退出。硬质支气管镜推进同时,需利用软质或者硬质管子不断清除气道分泌物,以充分保证操作视野干净。该方法适宜于初次操作者。
a b c
利用气管插管引导示意图
a:显示硬质支气管镜沿气管套管进入;b显示硬质支气管镜进入到声门上;c显示麻醉师将气囊放气后撤出气管套管
五、观察方法
硬质支气管镜进入气道后,通常先接上其远端的呼吸机接口进行机械通气,保持全身麻醉状态下有足够供氧。然后进一步观察左、右主支气管。如需进入右主支气管,则将患者头向左转,硬质支气管镜镜体缓慢旋转、推进通过窿突,多数情况下,可将镜的远端推进到中间支气管;如要进入左主支气管,则患者的头向右转,多数情况下可观察到上下叶支气管。一般杆状透镜视角为0º的硬质支气管镜的可视范围包括:气管、左、右主支气管和五个叶支气管的开口,而左上和右上叶的段支气管难以看到。如若要看到这些段支气管,一则可以换用有角度的目镜,或采用可屈支气管镜经硬质镜插入观察。完成操作后硬质支气管镜的移出应在直视下、在旋转移动中退出。
六、操作中通气方式和供氧
硬质支气管镜操作过程中通气方式有四种,自主呼吸、辅助性机械通气、控制性机械通气和手动式球囊按压。可以通过硬质支气管镜侧孔输入高流量空气或氧气。也可在镜体近端,通过特殊luer-lork孔进行高频喷射式通气。操作者应根据采用硬质支气管镜进行介入诊断及治疗目的和操作时间的不同,选择不同浓度的供氧和机械通气的方式。
取气道异物和进行支气管组织活检时,可以在数分钟内结束操作,建议吸入100%氧气,取出异物和取到组织后,再进行辅助机械通气等待患者苏醒。
气道内放置支架需要时间较长,自主呼吸较难以满足机体对氧的需求,特别是患者存在气道严重阻塞影响通气,此时,可以适当保留患者自主呼吸,应用辅助通气方式,呼吸频率由麻醉师控制。该方法优点为操作结束后患者可以很快苏醒;缺点为不能有效地控制操作过程中的咳嗽,可能出现支架放置错位或支架移位。放置支架既可以利用肌肉松驰剂和较深麻醉打断自主呼吸,给予控制性通气;也可采用高频喷射式通气,长时间维持操作过程中有效通气和气体交换。采用气体喷射率为50psi,建议提供100%氧气,同时监测经皮血氧饱和度。也有学者为减少供氧浓度,操作过程中为保持密闭通气,在口腔周围用纱布密封尽量减少漏气,该方法给操作带来不便,同时由于辅助呼吸时气道内压较高可能给患者带来气压伤的危险,控制漏气的方法可能更利用于采用吸入麻醉的方式。此外,也有先放置一内径较小的气管插管进行辅助或者控制性机械通气,然后沿插管旁插入硬质支气管镜进行操作,由于气道的局限性加上气道狭窄,给操作带来不便。笔者进行气道内支架置入时,强调与麻醉师密切配合,尽可能保留患者自主呼吸,充分气道内局部麻醉,尽可能抑制咳嗽反射,插入硬质支气管镜后给予100%氧气通气,允许短时间内气管镜保持开放,以尽快完成放置操作,同时监测经皮血氧饱和度,维持氧饱和度在90%以上,若氧饱和度降低,可暂停操作,接上呼吸机进行辅助或者控制通气,经过6年观察,支架置入操作过程中未出现因缺氧引起呼吸心跳骤停病例。
经硬质支气管镜进行激光治疗必须在全身麻醉状态进行。常规全麻后局麻,插入硬质支气管镜,从硬质支气管镜操作孔插入光导纤维及吸引管,目镜镜头、光导纤维及吸引管紧贴一起伸出硬质支气管镜远端开口,尽量靠近硬质支气管镜远端开口,直接对准目标或通过旋转硬质支气管镜准确定位后照射,待病变凝固后,通过吸引或活检钳清除坏死组织,也可利用硬质支气管镜远端斜面铲除病变,或旋转硬质支气管镜直接穿透阻塞部位疏通气管、支气管。由于气道内激光消融治疗操作时间较长,又由于氧燃烧等问题,气道内激光消融操作过程中的机械通气和氧供问题略复杂,笔者在为1例左主支气管肿瘤致管腔完全闭塞患者进行激光消融,整个操作时间长达8 h。为避免发生氧燃烧,应尽量注意进行激光消融治疗不同时吸氧;必须吸氧时,吸氧浓度应用低于40%。由于操作过程中需尽量避免给予高浓度的氧气,同时又由于坏死组织、出血、及分泌物阻塞气道,激光治疗过程中较易出现低氧血症时,就立即停止激光治疗并给高浓度氧,及时清除气道内道坏死组织及分泌物,或把硬质支气管镜直接穿过病变部位以通畅气道,必要时进行机械通气。此外,激光治疗过程中严密监测心电活动、血压和经皮血氧饱和度尤为重要,维持氧饱和度在 90%以上,可以明显减少由于缺氧引起的术后呼吸和心脏功能衰竭。
七、术中监测和术后麻醉苏醒
为减少操作过程中和术后呼吸和心血管并发症,减少病死率,进行必要监测至关重要。应用镇静剂时至少应连续监测经皮血氧饱和度情况。应用全身麻醉、神经肌肉松驰剂,应监测心电活动、呼吸运动、神志、血压和经皮血氧饱和度,在进行介入操作时,特别是在进行喷射式高频通气时,需经皮测定paCO2和paO2。严重的心脏功能不全患者在进行介入操作前,最好插入肺动脉导管监测心脏功能。
硬质支气管镜操作一般较为安全,并发症较少。 Caputi等报道11 000次硬质支气管镜操作过程中,2例患者死亡,硬质支气管镜操作引起的病死率不超过0.6%。笔者进行硬质支气管镜操作150余例,未出现1例死亡病例。但术后出现心功能衰竭3例,出现心肌梗死2例,考虑可能与患者年龄较大,存在冠状动脉潜在病变和操作时间过长有关。熟练技术和规范操作,是避免并发症死亡发生的关键。硬质支气管镜操作常见并发症有:
一、麻醉药物过敏或中毒
成人用1%地卡因表面浸润麻醉,可出现麻醉药物过敏,甚至出现变应性休克。因此在使用表面浸润麻醉前,应注意询问患者有无过敏史,第一次喷药量宜少,观察无异常反应后,再按麻醉要求用药。同时应严格控制麻醉药的用量,卡地因总量不应超过60 mg,利多卡因总量不超过400 mg,以免引起麻醉药物中毒。小儿全身麻醉,因麻醉过深可引起中毒,目前此种并发症已少见,但仍应谨慎。
二、口腔损伤
硬质支气管镜检查时,将上唇挤压在镜管与牙齿之间,易造成上唇损伤,手术应将上唇推开避免损伤。此外硬支镜检查时如以切牙作为支点,可引起切牙松动或脱落。因此手术时应避免以切牙作为支点。
三、声带损伤及杓状软骨脱位
多因操作者对解剖不熟悉或操作不细致引起。检查者在未看清声带及杓状软骨的情况下,盲目推进硬质支气管镜,以致造成声带损伤及杓状软骨脱位。尤其是在紧急情况下更易发生。故手术者必须熟悉解剖,手术时必须按操作规程进行,在未认清标声前,不应盲目将镜管向前推进。
四、喉水肿
多见于小儿,因小儿喉部黏膜下组织疏松,淋巴组织丰富。手术时操作粗暴易损伤喉组织,手术操作时间过长或支气管镜太粗等,均可刺激喉部发生喉水肿。预防的方法是避免以上原因,手术尽量使用全身麻醉。术中及术后,重复肌注或静注地塞米松5 mg,对预防喉水肿有一定作用。
五、喉痉挛
无麻醉或麻醉太浅,在挑起会厌暴露声门时,可刺激声门引起喉痉挛。喉痉挛也可以发生在支气管镜退出声门后。因此特别强调无论是局麻或全麻患者在支气管镜插入过程中,逐步喷入1%地卡因,尤其是声门区。支气管镜检查完毕退至声门区,亦应喷入1%地卡因,以防发生喉痉挛。
六、窒息
多发生在取异物过程中,异物堵塞部位发生改变,一侧或两侧支气管发生完全阻塞,以致引起窒息,尤其是已有一侧肺不张或肺气肿情况下,异物又堵塞健侧肺部,更易发生窒息。遇此情况,检查者必须慎重而快速地首先取出健侧异物,然后再取出患侧异物。
七、咯血
使用支气管镜或异物钳用力不当或方向不正确,均可损伤黏膜,引起咯血;吸引管负压过大,也可损伤黏膜,尤其是小儿。所以小儿吸引管应是两侧开口或将吸引器开至最小档,减少吸引力,避免损伤黏膜。
八、支气管破裂或支气管嵴损伤
很少见,但支气管镜插入时,镜轴与支气管不在一条直线上;或钳除异物时,钳住支气管壁及支气管嵴,造成支气管破裂穿孔,甚至发生纵隔气肿及气胸,引起严重并发症。因此在钳取异物后应缓慢退出,若感觉拉力很大,且钳取物随呼吸运动而上下运动,则应放松钳取物,重新钳取,以免损伤支气管壁。
一、气道异物的摘除
从硬质支气管镜问世到20世纪60年代,摘除呼吸道异物一直是其最主要的适应证,尤其适用于儿童患者,通常异物位于大气道且体积较大。儿童气道结构尚未发育成熟,咳嗽反射弱,呼吸道异物发生率明显高于成人。Kruk等总结了1945年~1997年间,237例下呼吸道异物患者中,年龄在0~10岁者占80%,异物存在最长时间为18年,约98%经硬质支气管镜摘除,未见明显并发症。对成人患者,大多数医生首选纤支镜,如果前者失败,才考虑使用硬质支气管镜。使用纤支镜时,若患者配合差,容易损伤镜子并容易造成低氧血症危及生命。而硬质支气管镜由于配有机械通气接口,患者全身麻醉后连接呼吸机,能够有效维持呼吸功能,安全性高,操作效果好。 Martinot等回顾了83例可疑有气道异物儿童患者的临床表现及治疗结果,28例儿童先作硬质支气管镜,23例阳性;55例先作纤支镜,17例阳性,他们认为如果患者出现呼吸困难、单侧呼吸音减低、阻塞性肺气肿、影像学可疑气道异物四种表现时,可首选硬质支气管镜。标准支气管镜异物钳及光学异物钳(optical forceps)是目前常用的两种钳子,Hilmi等通过随机实验对比,发现两者效果无明显差异。
二、气道狭窄的介入治疗
治疗气道狭窄是硬质支气管镜另一主要适应证。肺癌等恶性肿瘤是造成气道狭窄的主要原因,吸入性烧伤、支气管内膜结核、气管插管及气管切开后瘢痕增生、支气管软化征等良性疾病造成的狭窄也时有发生。放置支架是解决气道狭窄的重要方法,通常放置硅胶支架或用来治疗双侧主支气管狭窄或气管隆突旁病变的Y形支架需要使用硬质镜,与纤支镜相比,硬镜管腔大、视野清晰、通气保证,操作方便、时间短、放置位置较准确,特别是对气管严重狭窄的患者,硬质支气管镜的优势更加明显。支架置入后可以减轻呼吸困难,更为进一步腔内治疗如电凝、微波烧灼、后装放疗、球囊扩张等创造了条件。对于一些良性的气道瘢痕狭窄,在硬质支气管镜下采用扩张探条进行扩张也可收到较好的疗效。氩气刀(argon protein coagulation, APC)是一种新兴的介入治疗手段,Reichle等用APC技术为186例恶性肿瘤造成气道狭窄患者治疗,90%的操作在硬质镜下完成,有效率约 67%。Daddi等为304例因恶性肿瘤造成气道狭窄的患者,行硬质镜下介入治疗,腔内肿瘤的手术切除率达95%。气道再狭窄是肺移植后一个严重而常见的并发症,Lonchyna等于1994~1997年间在硬质镜下为107例肺移植患者进行球囊扩张,放置支架,成功率100%,未发生严重并发症。
三、大咯血的治疗
硬质支气管镜下治疗大咯血较可弯曲支气管镜更安全、有效。由于硬质支气管镜管腔大,出血部位显露清晰,吸引器导管粗,可迅速吸出气道血液,并同时可以辅助通气,尤其对于迅速、大量的气道出血更为适用。硬质镜压迫管壁可起到止血作用。咯血相对控制后,可再将纤支镜插入硬质镜检查远端气道,明确出血部位并进一步治疗。体外循环过程中出现的大咯血,出血量大,速度快,易造成窒息。Smythe等报道3例患者体外循环时出现大咯血,经硬质镜清除积血和立即停止体外循环等抢救后,2例存活,1例死亡,认为快速使用硬质支气管镜维持通气,是抢救成功的关键。
四、其他
硬质镜下可便于机械性切除气道肿瘤。Fan等用硬质镜治疗右肺不张造成纵隔移位的危重早产儿,清除痰栓或分泌物,冲洗阻塞气道,受累肺叶可得到完全复张,再给予间歇性高频喷气通气,疗效显著。支气管软化症、支气管结石、支气管畸形、肺脓肿、支气管结石症、原发性气道淀粉样变等均可在硬质镜下获得有效治疗。