
2016-10-04
肿瘤转移是指肿瘤细胞在病人体内从原发部位向远处播散,到达继发组织或器官后得以继续增殖生长,形成与原发肿瘤相同性质的继发肿瘤的全过程。
肿瘤转移是恶性肿瘤生物学特征之一,不同肿瘤的转移能力不同:
当黑色素瘤侵犯进入皮下组织时,癌细胞扩散至机体远端已成定局。
皮肤鳞状细胞癌、脑星状细胞瘤则很少发生转移
肿瘤转移的危害
原发肿瘤只引起10%的肿瘤患者死亡,80%-90%以上的肿瘤患者死于侵袭和转移。
例如乳腺癌:
局限于乳腺的原发瘤不会威胁生命
脑转移:损伤中枢神经
肝、肺转移:影响器官功能
骨转移:骨组织局部侵蚀
60%以上的恶性肿瘤患者于初诊时已发现有转移。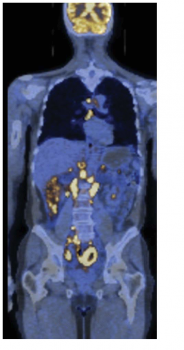
转移性淋巴瘤的PET-CT扫描图
肿瘤转移的方式
淋巴管、血管和种植等途径是肿瘤转移的常见方式。
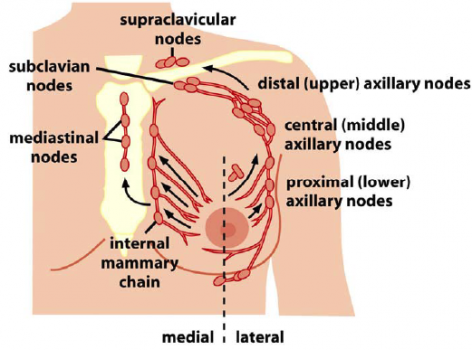
淋巴管转移:
● 上皮组织来源的恶性肿瘤多经淋巴道转移。
● 癌细胞侵入淋巴管后,首先到达局部淋巴结,继续增殖发展为淋巴结内转移瘤。转移瘤自淋巴结边缘开始生长,逐渐累及整个淋巴结。有时由于
瘤组织侵出被膜而使多个淋巴结相互融合成团块。例如乳腺癌常先转移到同侧腋窝淋巴结。
● 局部淋巴结转移后,可继续转移至下一站淋巴结,也可进入血流再发生血道转移。临床上最常见的癌转移淋巴结是左锁骨上淋巴结,其原发部位多位
于肺和胃肠道。
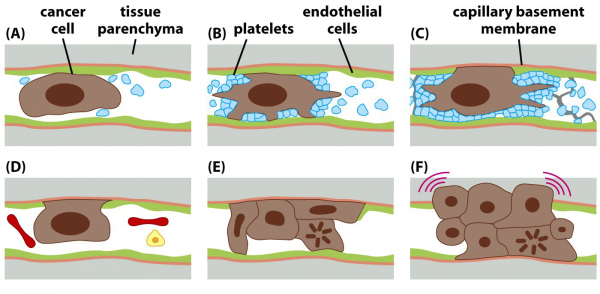
血道转移:
● 各种恶性肿瘤;
● 突破基底膜前,肿瘤细胞分泌促血管生长因子刺激血管生成。突破基底膜后,肿瘤细胞可以突破管壁进入血管和淋巴管,这一侵入血管的过程称为内渗。
● 癌细胞经毛细血管与小静脉直接入血;或经淋巴管-胸导管或淋巴—静脉通路入血;
● 进入血管系统的癌细胞常与纤维蛋白及血小板共同粘聚成团,称为癌栓,可阻留于靶器官的小血管内,由此介导内皮细胞发生变性,癌细胞可自内皮损伤处或内皮之间穿出血管,进入组织内增殖,形成转移癌。
● 经血道可转移至许多器官,但最常见的是肺,其次是肝、骨、脑。
种植性转移:
● 当癌细胞侵及体腔器官表面时,可以脱落并种植在体腔内各器官的表面甚至侵入其下生长,形成转移癌。如胃癌破坏胃壁侵及浆膜后,可在腹腔和盆腔脏器表面形成广泛的种植性转移。肺癌常在胸腔形成广泛的种植性转移。脑部恶性肿瘤,如小脑的髓母细胞瘤亦可经过脑脊液转移到脑的其他部位,形成种植性转移。
● 经体腔转移常伴有体腔积液和脏器间的癌性粘连。积液多为血性,其内含有脱落的癌细胞,可供细胞学检查。
● 值得注意的是穿刺检查也可能造成医源性种植。
肿瘤多步骤转移过程
1. 早期原发癌生长: 肿瘤细胞生长所需养料由组织器官微环境渗透提供。
2. 肿瘤血管生成: 肿瘤直径超过1-2mm时,新生血管逐步形成。
3. 肿瘤细胞侵袭基底膜和细胞外基质:细胞间以及细胞与细胞外基质黏附能力下降,在蛋白酶溶解作用下破坏基底膜和细胞外基质。
基底膜是由不同的蛋白纤维组成的网状结构,位于上皮细胞基底面与结缔组织之间,具有支持连接作用,亦是物质通透的半透膜。
4. 进入脉管系统:肿瘤组织的血管与正常血管差异显著。进入血液循环的肿瘤细胞大部分被杀死,只有少数转移倾向极高的细胞相互聚集形成微小癌栓存活。
5. 特定组织器官定位生长:癌细胞到达特定的组织器官,通过特异性锚定在毛细血管壁上,穿透管壁进入周围组织,并逃避宿主的局部非特异性免疫杀伤作用,最终形成肿瘤转移灶。
6. 转移癌继续扩散
肿瘤转移基本过程的总结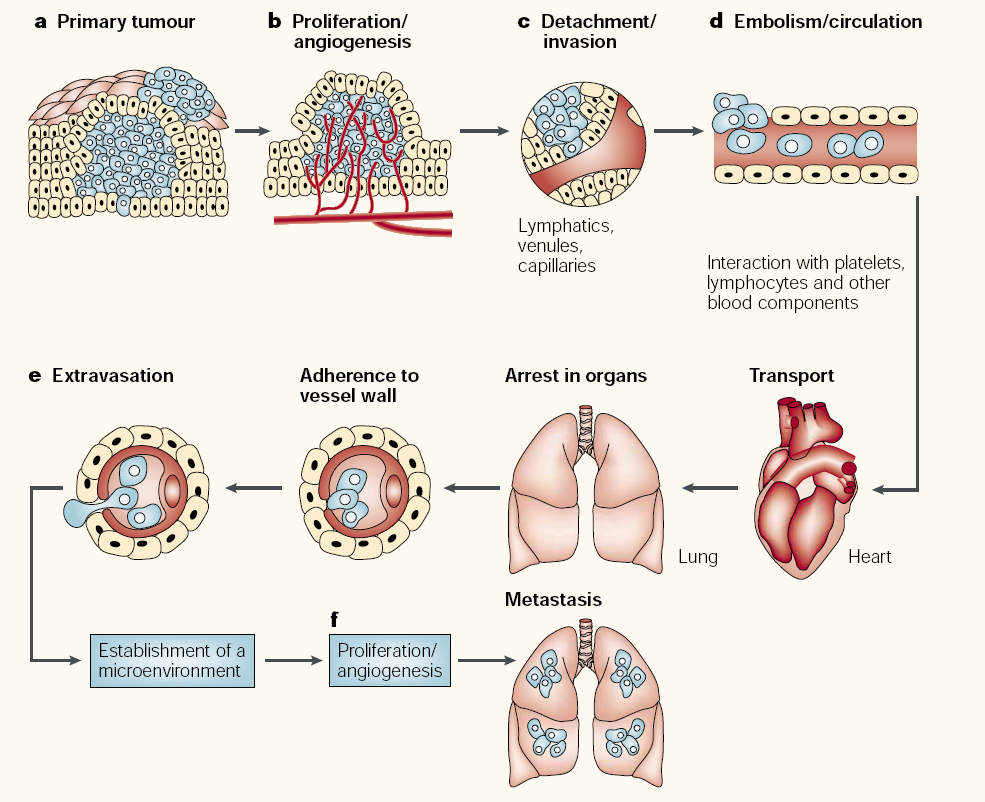
肿瘤转移的器官选择性及其影响因素
区域性播散,如区域淋巴结转移,主要受机械和解剖因素影响;
远处转移则具有器官选择性的特点。
影响器官选择性的主要因素:
● 肿瘤表型的差异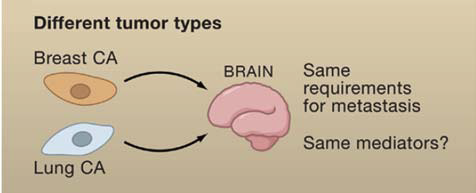
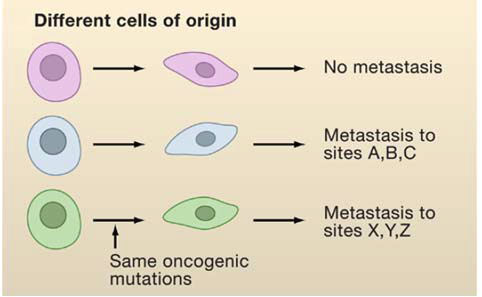
● 微环境
肿瘤细胞通过与宿主细胞相互作用改造微环境,其最终生长状态取决于微环境自分泌、旁分泌和内分泌产生的正性和负性生长信号间的综合平衡。器官微环境内转移介质分子如生长因子,黏附因子和驱化因子与肿瘤转移器官选择性关系密切。
运动能力的获得
为获得运动和侵袭能力,肿瘤细胞必须丢失许多上皮细胞表型,使上皮层发生巨大改变---上皮间叶转变(epithelial-mesenchymal transition, EMT)
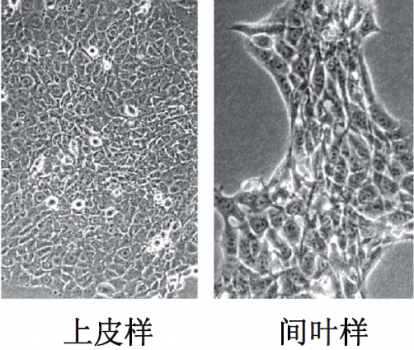
● 细胞形态改变
上皮样细胞:鹅卵石型、运动能力差
间叶样细胞:梭型、运动能力强
● 获得运动能力
● 基因表达谱改变
转移克隆的起源
1 、肿瘤异质性理论:恶性肿瘤具异质性,由血管生成、侵袭能力、转移特性等方面不同的细胞亚群组成,其中仅有少数细胞具有转移潜能。肿瘤转移潜能的获得是多步骤、逐渐改变的过程,且肿瘤转移发生在肿瘤进展的晚期。
2 、克隆优势学说:在肿瘤形成的早期具有转移潜能的细胞亚群就已形成生长优势,逐渐成为原发肿瘤中的优势细胞群体。转移细胞克隆来源于原发肿瘤总的遗传易感性,而非个别具有转移潜能的变异克隆。
影响转移过程的因素
1、肿瘤血管生成
2、黏附分子:
3、MMPs/TIMPs蛋白酶系统:
4、肿瘤微环境:
黏附分子
肿瘤细胞要产生转移首先必须降低细胞间的粘附,破坏细胞与细胞外基质的联系,使得细胞从原发灶脱落,然后游走并进入血管或淋巴管。
黏附因子(cell-adhesion molecules, CAM)是一类介导细胞与细胞、细胞与胞外基质间粘附作用的膜表面糖蛋白。
● 细胞与细胞间的黏附:
同源细胞间的粘附:如E-钙粘连素(E-cadherins) ,
异源细胞间的黏附:如选择素(selectin) ,介导肿瘤细胞与血小板、内皮细胞和基质细胞的结合。
● 细胞与细胞外基质的黏附:整合素(integrins)
MMPs/TIMPs蛋白酶系统
基质金属蛋白酶(matrix metalloproteinases, MMPs) :锌离子和钙离子依赖的蛋白水解酶,主要功能是降解细胞外基质和基底膜大分子。根据其对底物的特异性和结构分为五大类:胶原酶( collogenases)、明胶酶( gelatinase) 、基质溶解素(stromelysins)、膜性MMPs (MT-MMPs)
MMPs对肿瘤转移的影响
● 降解细胞外基质(ECM)
ECM尤其是基底膜是肿瘤转移过程中必须克服的生理屏障,每种MMP均有其降解的底物。
● 调节细胞黏附
MMP-3和MMP-7均可水解E-钙连接蛋白。
● 促进新生血管形成
上皮细胞明胶酶即MMP-2和MMP-9降解血管基底膜和细胞间的胶原,是肿瘤血管形所必需的。
基质金属蛋白酶组织抑制剂(tissue inhibitors of matrix metalloproteinases, TIMPs )
● TIMPs作为MMPs的天然抑制剂可下调MMPs的活性。
● TIMPs主要从两个方面抑制MMPs的激活:
TIMPs与酶原形成复合物,阻碍酶原的自我激活;
TIMPs与活化状态的MMPs以1∶1分子比例稳定地结合,从而抑制MMPs的活性。
肿瘤组织中的基底膜
正常上皮组织结构不利于恶性肿瘤细胞的运动和侵袭
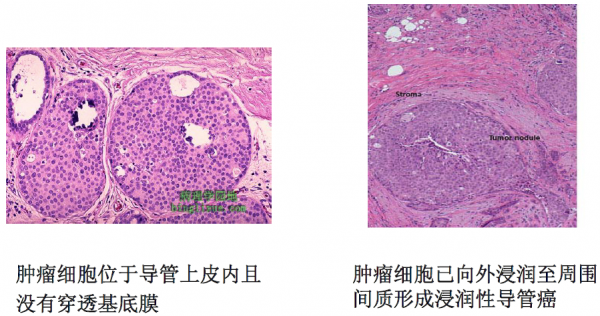
良性肿瘤:来源于基底膜上皮侧并局限于这一侧的肿瘤
恶性肿瘤:单个或一群肿瘤细胞获得穿透基底膜的能力,侵入邻近的基质
肿瘤细胞侵袭基底膜和细胞外基质
● 细胞间黏附能力下降
● 细胞与细胞外基质黏附能力下降
● 蛋白酶溶解、破坏基底膜和细胞外基质
肿瘤微环境
● 基质细胞:如成纤维细胞、上皮细胞、脂肪细胞、免疫细胞和血管内皮细胞等
● 细胞外基质:extracellular matrix,ECM
● 细胞外分子:如ERF、VEGF、FGF、TGFβ等
微环境与肿瘤细胞的相互作用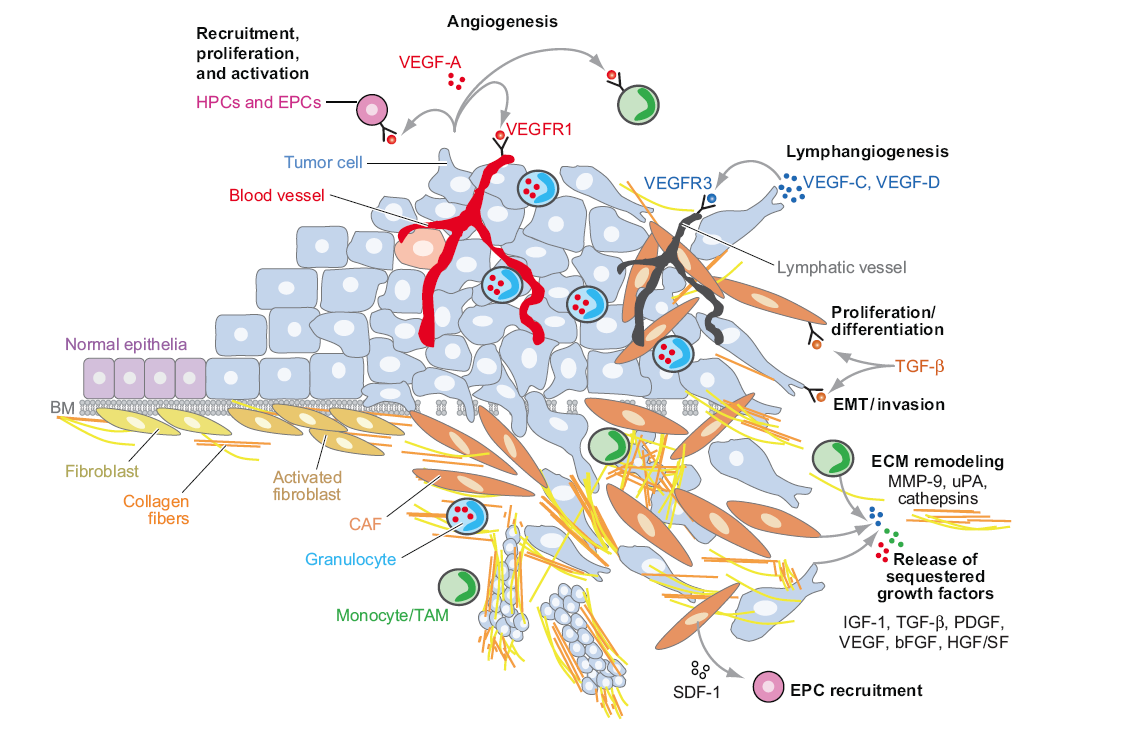
克隆形成
一旦转移的肿瘤细胞到达实质组织,它们将在新的环境中增殖并形成肿瘤团块,这个过程称为克隆形成,这是侵袭‐转移级联反应的限速步骤。
例如,30%的乳腺癌患者骨髓中有成千上万的微转移灶,但仅有其中的一半患者由于大转移灶的形成而复发疾病。
微小转移灶生长成为大转移灶是形成转移疾病的关键步骤。
隐匿性微小转移灶可以长期处于生长静止的休眠状态。单个隐匿性乳腺癌细胞可以在肝脏存活数周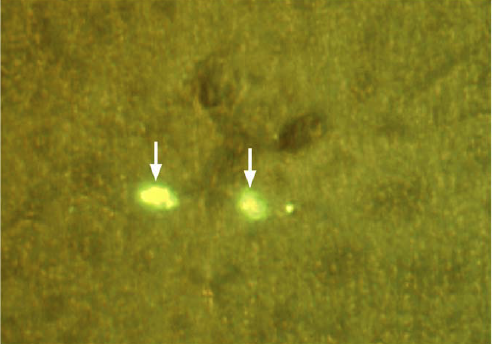
将荧光标记的肿瘤细胞注射入肠系膜静脉,11周后检测肝脏中荧光信号
癌细胞在特定组织形成克隆的能力具有高度特异性
● 5%的乳头状甲状腺癌患者有明显的淋巴结转移,很少发生远处转移
● 十二指肠癌具有高频率的淋巴结转移,但少转移至肝
● 结肠癌常发生肝转移,如果切除孤立的结肠癌肝转移灶,有利于延长患者无疾病进展生存期
原发瘤及其转移定向性
● 区域性播散,如区域淋巴结转移,主要受机械和解剖因素影响;
● 远处转移则具有器官选择性的特点。
转移至器官的概率一般由两个参数决定:
转移的癌细胞被组织捕获的概率
癌细胞适应组织微环境并形成克隆的能力
影响器官选择性的主要因素
组织微环境:肿瘤细胞通过与宿主细胞相互作用改造微环境,其最终生长状态取决于微环境自分泌、旁分泌和内分泌产生的正性和负性生长信号间的综合平衡。例如:淋巴结、骨及肺等部位表达趋化因子CXCL12,乳腺癌高表达其受体CXCR4,CXCL12能趋化乳腺癌细胞,并能其促使伸出伪足。
转移克隆的起源
● 肿瘤异质性理论
● 克隆优势学说
肿瘤异质性理论
● 恶性肿瘤具异质性,由促血管生成、侵袭能力、转移特性等方面不同的细胞亚群组成,其中仅有少数细胞具有转移潜能。
● 肿瘤转移潜能的获得是多步骤、逐渐改变的过程且肿瘤转移发生在肿瘤进展的晚期。
克隆优势学说
在肿瘤形成的早期具有转移潜能的细胞亚群就已形成生长优势,逐渐成为原发肿瘤中的优势细胞群体。转移细胞克隆来源于原发肿瘤总的遗传易感性,而非个别具有转移潜能的变异克隆。
作者:健康全记录
推荐阅读
文章评论
注册或登后即可发表评论
登录/注册
全部评论(0)