
2019-03-06
题目
[NADIM研究]可切除的IIIA期NSCLC新辅助化疗联合免疫治疗
背景
IIIAN2非小细胞肺癌的预后差,5年生存约10%-15%。在未选择的转移性NSCLC患者中,化疗联合免疫可以有效提高客观缓解率,延长总生存。在新辅助治疗阶段,这一联合方案的疗效如何,目前未知。
新辅助两个剂量纳武利尤单抗(nivolumab)在早期肺癌病人中可以达到显著病理缓解(major pathologic response,mPR。定义是<10%的肿瘤细胞)。
方案
NADIM研究(CA209-547 , NCT03081689 )是一项II期,单臂,开放的多中心研究,入组局部晚期可切除的IIIA N2期NSCLC 患者。患者接受化疗联合纳武利尤单抗治疗序贯附属治疗1年。新辅助治疗方案包括3个周期的纳武利尤单抗360mg IV Q3W 联合紫杉醇(paclitaxel)200mg/m2和卡铂(carboplatin)AUC6 IV Q3W化疗。在完成新辅助治疗后,手术前进行肿瘤评估。在完成3个周期的新辅助治疗后的第3或4周进行手术。辅助治疗方案为纳武利尤单抗240mg IV Q2W,4个月和纳武利尤单抗480mg IV Q4W,8个月,术后辅助治疗共12个月。研究计划招募46例患者。主要研究终点为从诊断计算起的24个月的无进展生存(progression-free survival,PFS率。太奇怪了吧,是手术的病人,为什么不是无疾病生存呢?)。采用客观病例缓解标准进行疗效探索性分析。本次报道完成了3个周期新辅助治疗后接受手术治疗患者的初步研究数据。
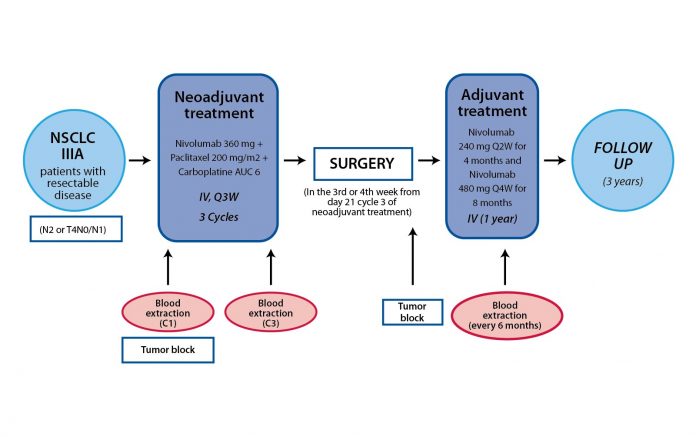
图1. NADIM: 研究设计和流程
结果
截至递交数据,研究共纳入46例患者,其中30例患者完成手术。化疗联合免疫治疗的耐受性良好,所有病例都能够依从方案,没有患者延长进行守护。没有患者因为基本进展或毒性在术前需要退出研究。共进行了20例手术,所有肿瘤均为可切除的。
具体的药物方案实施见: 纳武利尤单抗+紫杉醇+卡铂(NADIM方案)
疗效评价RECIST v1.1并以CT扫描评价。总体临床缓解率评估中,70%有效(21/30),3例CR(10%),18例PR(60%),9例(9/30,30%)SD稳定。90%出现降期。
术后病例缓解率评估中,13例(65.0%;95% CI 40.8-84.6%) 患者取得病理完成缓解,3例(3/30,10%)患者取得大的病理缓解,定义为切除标本中存活肿瘤细胞<10%。结合取得完全病理缓解和大PR的患者,总的ORR为80.0% (95% CI 56.3-94.3%),CR率为60%。
毒性均可耐受。mPR在本研究中很高。
未报道术中并发症,但术后有7/30例术后并发症,但无术后死亡率。
结论
这是第一项多中心研究,在新辅助治疗阶段评估化疗联合免疫治疗,在局部晚期,潜在可切除的NSCLC患者中显示出卓越的抗肿瘤疗效,达到了超过预期的病理完全缓解率。
评论
在III期NSCLC中,这个mPR是前所未有的高!!!!!!但进入III期临床试验还要有3年才能等到结果NADIM II: Neo-Adjuvant Immunotherapy (NADIMII)。
存在的问题
待讨论。
相似的研究
NADIM II: Neo-Adjuvant Immunotherapy (NADIMII)
AFT-16 (NCT03102242) :
单臂,II期研究。III期非小细胞肺癌。
治愈性化放疗前后atezolizumab治疗。预计入组63列。
Ross HJ, Kozono DE, Urbanic JJ, et al. Phase II trial of atezolizumab before and after definitive chemoradiation for unresectable stage III NSCLC. J Clin Oncol 2018;36:abstr TPS8585.
SAKK 16/14 (NCT02572843):
单臂,II期研究。IIIA期 (N2) 非小细胞肺癌。
新辅助 顺铂+多西他赛3周期,加2周期durvalumab,手术后再加术后辅助durvalumab 12个月。入组68例。主要终点:无事件生存12个月。
25例手术,30天术后死亡率<10%。
Rothschild SI, Zippelius A, Prince SS, et al. SAKK 16/14 - anti-PD-L1 antibody durvalumab (MEDI4736) in addition to neoadjuvant chemotherapy in patients with stage IIIA (N2) non-small cell lung cancer (NSCLC). A multicenter single-arm phase II trial. J Clin Oncol 2018;36:abstr TPS8584.
EA5142 (ANVIL; NCT02595944):
ALCHEMIST的一部分,III期试验,随机入组714例,辅助nivolumab对比标准治疗。病理证实的IB–IIIA NSCLC。
Chaft JE, Dahlberg SE, Khullar OV, et al. EA5142 adjuvant nivolumab in resected lung cancers (ANVIL). J Clin Oncol 2018;36:abstr TPS8581.
Checkmate-816 (NCT02998528):
III期试验。
新辅助nivolumab + ipilimumab 对比 新辅助含铂双药物化疗, IB–IIIA NSCLC. 入组326例。
主要终点:major pathological response rate。
Forde PM, Chaft JE, Felip E, et al. Checkmate 816: A phase 3, randomized, open-label trial of nivolumab plus ipilimumab vs platinum-doublet chemotherapy as neoadjuvant treatment for early-stage NSCLC. J Clin Oncol 2017;35:abstr TPS8577.
作者:广东省肺癌研究所 杨学宁 & LAMP
参考文献
1. Mariano Provencio-Pulla, MD, PhD Neoadjuvant Nivolumab Shows Unprecedented Pathologic Complete Response for Stage III NSCLC
2. Provencio-Pulla M, Nadal-Alforja E, Cobo M, et al. Neoadjuvant chemo/immunotherapy for the treatment of stages IIIA resectable non-small cell lung cancer (NSCLC): A phase II multicenter exploratory study—NADIM study-SLCG. J Clin Oncol 2018;36:abstr 8521.
3. Langer CJ, Leighton JC, Comis RL, et al. Paclitaxel and carboplatin in combination in the treatment of advanced non-small-cell lung cancer (NSCLC): A phase II toxicity, response, and survival analysis (FCCC 93-024). J Clin Oncol. 1995;13(8):1860-1870.
4. Forde PM, Chaft JE, Smith V, et al. Neoadjuvant PD-1 blockade in resectable lung cancer. N Engl J Med. 2018;378(21):1976-1986.
5. Sugarbaker DJ, Herdon J, Kohman LJ, et al. Results of cancer and leukemia group B protocol 8935: A multi-institutional phase II trimodality trial for stage IIIA (N2) non-small-cell lung cancer-Cancer and Leukemia Group B Thoracic Surgery Group. J Thorc Cardiovasc Surg. 1995;109(3):473-485.
6. Kirn DH, Lynch TJ, Mentzer SJ, et al. Multimodality therapy of patients with stage IIIA, N2 non-small–cell lung cancer: Impact of preoperative chemotherapy on resectability and downstaging. J Thorac Cardiovasc Surg. 1993;106(4):696-702.
7. Choi Y S, shim Y M, Kim J, Kim K. Recurrence-free survival and prognostic factors in resected pN2 non-small cell lung cancer. Eur J Cardiothorac Surg. 2002;22(5):695-700.
8. Hellmann M, Chaft JE, William WN, et al. Pathologic response after neoadjuvant chemotherapy in resectable non-small lung cancers: proposal for the use of “major pathologic response” as a surrogate endpoint. Lancet Oncol. 2014;15(1):e42-e50.
9. Martini N, Kris MG, Flehinger BJ, et al. Preoperative chemotherapy for stage IIIa (N2) lung cancer: The Sloan-Kettering experience with 136 patients. Ann Thorc Surg.
10. Martín N. Mediastinal lymph node dissection for lung cancer: The Memorial experience. Chest Surg Clin N Am. 1995;5(2):189-203.
推荐阅读
文章评论
注册或登后即可发表评论
登录/注册
全部评论(0)