
2019-03-18
作者:广东省肺癌研究所

肺癌是世界范围内致死率最高的肿瘤,每年约有160万肿瘤病人死于肺癌,有51%的肺癌发生来自亚洲人群,致死率方面亚洲人群占据21%的比例。2018年ESMO更新了对晚期非小细胞肺癌进行诊断、治疗以及随访的临床实践指南,考虑到种族差异,ESMO与CSCO于2017年ESMO Asia会议上共同决定发布一份基于ESMO 2018指南、专门针对亚洲人群的晚期非小细胞肺癌临床指南,该指南代表来自中国、日本、韩国、马来西亚、新加波以及台湾六大国家或地区肿瘤学会(CSCO, JSMO, KSMO, MOS, SSO and TOS)的临床肿瘤学专家们的共识。
共识达成过程:
专家们对ESMO于2018年更新的临床实践指南中的topics及建议予以判断是否同样适用于亚洲地区,并给出有科学证据支持的理由;在此基础上,专家们聚集广州进行最终投票。

本次共识指南包括以下24类:
1. 诊断;2. 病理/分子检测;3. 分期及风险评估;4. 晚期病人的管理;
5. 无可驱动基因的一线治疗;6. 维持治疗;7. PS评分大于等于2的病人治疗;
8. 老年病人治疗;9. 无可驱动基因的二线治疗;10. EGFR突变的一线治疗;
11. EGFR突变的二线治疗;12. ALK重排的一线治疗;13. ALK重排的二线治疗;
14. ROS1重排的治疗;15. BRAF突变的治疗;16. 有其他可驱动基因的治疗;
17. 放疗的地位;18. 脑转移;19. 脑膜转移;20. 寡转移的治疗;21. 骨转移;
22. 微创手术在晚期肺癌的地位;23. 姑息治疗;24. 随访
Summary of final recommendations by Asian experts
1. 诊断:
中央型病灶建议气管镜活检;区域淋巴结建议EBUS;中间及外周型病灶建议经皮穿刺肺活检;胸腔穿刺术可同时作为诊断手段及姑息治疗;前面的活检手段不适用时,可考虑采用侵入性的手术方式(纵隔镜、纵隔切开术、胸腔镜);穿刺前病理科医生及操作者共同决定穿刺方式。
2. 病理/分子检测:
需获取足够的肿瘤组织行病理及分子检测,病理诊断需基于2015年WHO的肺癌分类;尽可能降低NSCLC-NOS的诊断率;EGFR/T790M/ALK/ROS1/BRAFV600/PD-L1 IHC必须检测;鳞癌病人不推荐EGFR/ALK基因检测,除外非吸烟者等特殊情况;可优先考虑多元化平台行分子检测。
3. 分期及风险评估:
需记录完整病史包括吸烟史、既往史、体重变化、PS及体格检查;血液检测、增强胸腹CT必须实行;血清肿瘤标志物不做常规推荐;脑部检查在晚期NSCLC予以推荐,有神经症状的则必须实行;骨扫描或PET建议用于骨转移的诊断;分期应基于AJCC/UICC系统第八版;单病灶转移需有病理的支持诊断;每6-9周行一次疗效评估;不推荐PET作为随访检查;评估标准采用RECIST。
4. 晚期病人的管理:
治疗决策需基于组织学类型、分子检测结果、年龄、PS评分、并发症及病人的意见;PS评分0-2的病人需接受系统治疗;所有的NSCLC均建议戒烟。
5. 无可驱动基因的治疗:
晚期鳞癌的治疗建议:
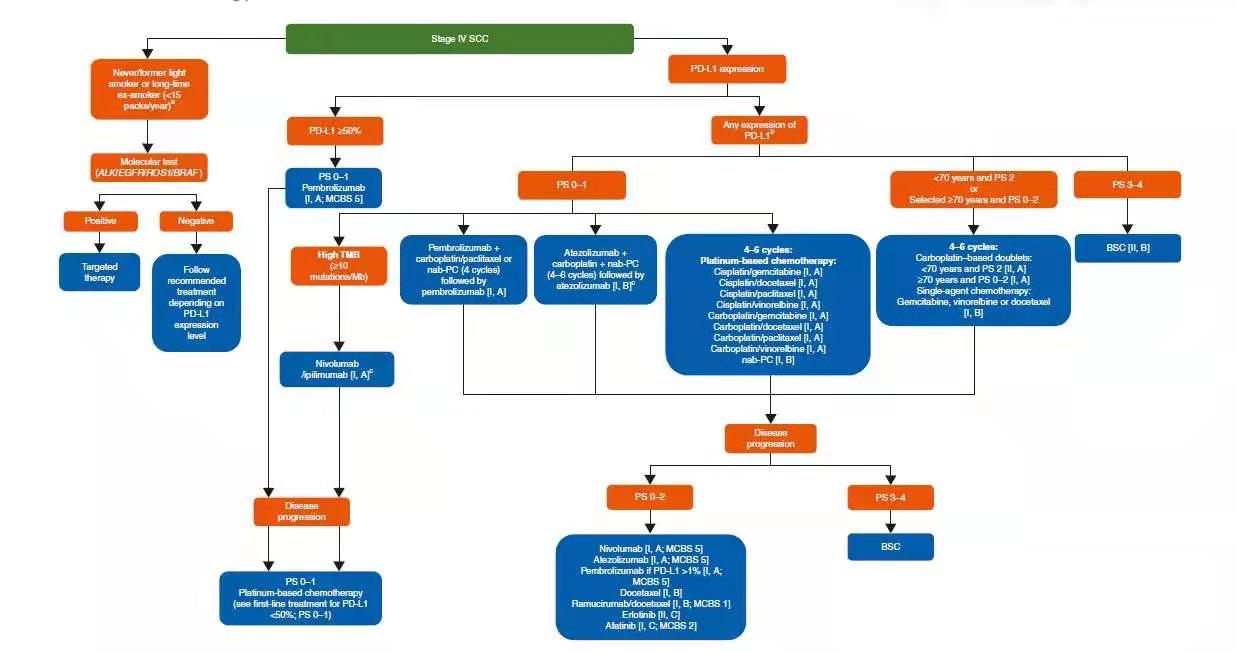
轻度吸烟患者建议行基因检测;所有鳞癌患者均建议做PD-L1的检测;无任何驱动基因的鳞癌,若PD-L1大于50%,建议一线使用Pembrolizumab,二线使用化疗;无任何驱动基因的鳞癌,无论PD-L1的表达情况,一线可选择方案包括:Pembrolizumab+化疗、Atezolizumab+化疗、单纯化疗,二线使用化疗;TMB高的(>10 mutations/Mb),建议一线使用Nivolumab。
晚期、无可驱动基因(EGFR/ALK/ROS1/BRAF)、肺腺癌的治疗建议:
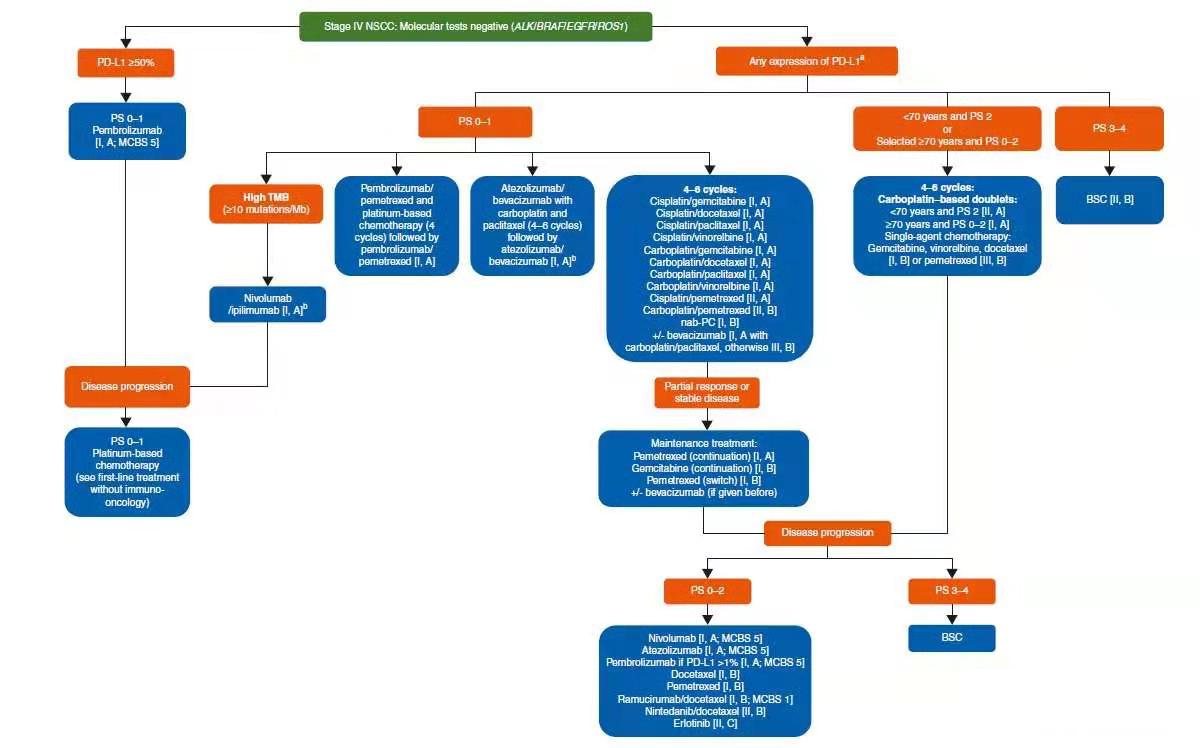
所有无可驱动基因的腺癌患者均建议做PD-L1的检测;若PD-L1大于50%,建议一线使用Pembrolizumab,二线使用化疗;无论PD-L1的表达情况,一线可选择方案包括:Pembrolizumab+化疗、Atezolizumab+化疗、单纯化疗;TMB高的(>10mutations/Mb),建议一线使用Nivolumab;若一线单纯使用化疗PCB的方案后疗效为PR/SD,可予培美曲赛等维持治疗,进展后二线可推荐Nivolumab或者Atezolizumab或者Pembrolizumab或者化疗等;无驱动基因或驱动基因未明确的病人暂不予推荐靶向二线或三线治疗。
6. 针对EGFR突变的治疗建议:
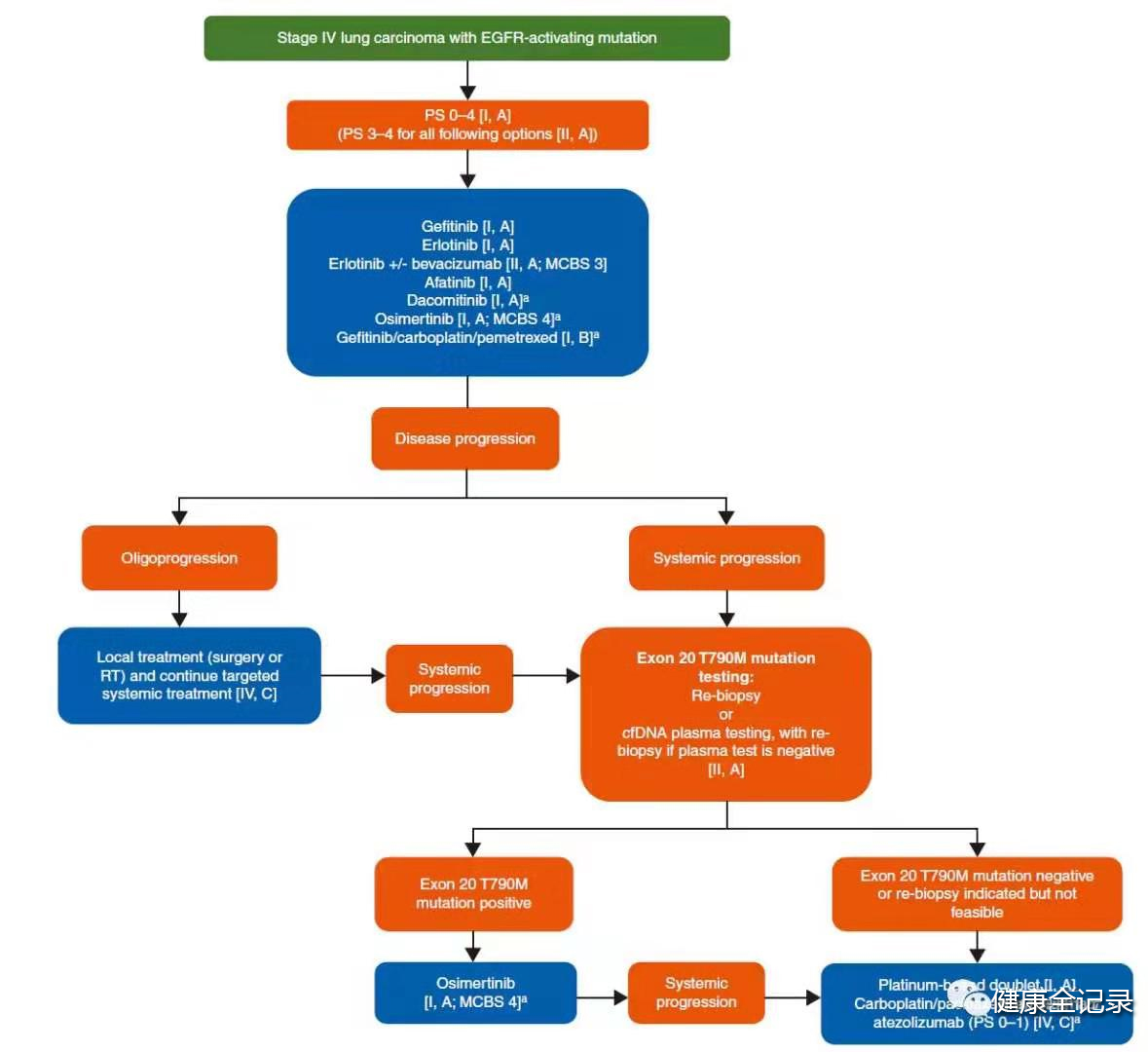
EGFR突变的病人可选的一线治疗方案包括:Erlotinib/Gefitinib/Afatinib/Dacomitinib/Osimertinib/Erlotinib+bevacizumab;一线治疗若出现局部进展,可对寡转移部位行局部干预;一线治疗若出现全身进展,T790M阳性的予以Osimertinib,T790M阴性的予以化疗。
7. ALK/ROS1/BRAF突变的治疗建议:
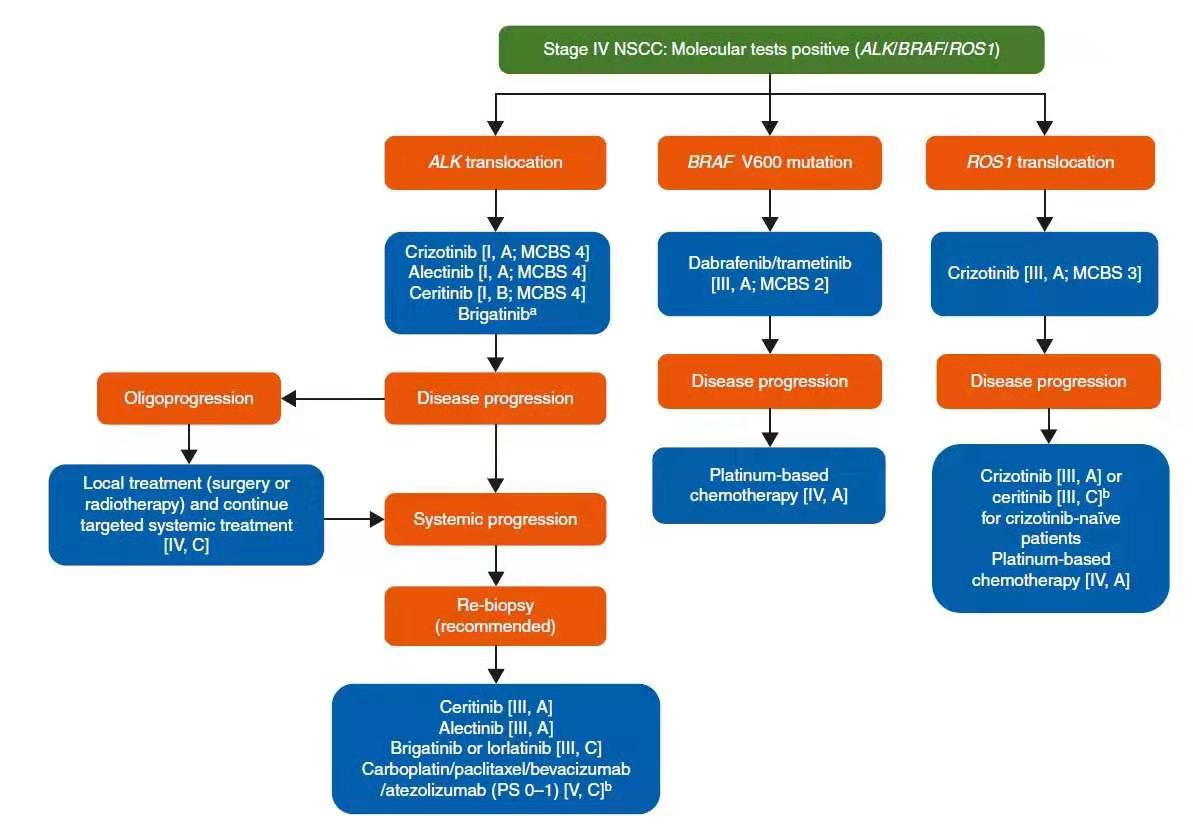
ALK重排的病人一线可选择方案包括:Crizotinib/Alectinib/Ceritinib/Brigatinib,一线治疗全身进展后,可选择方案包括:Ceritinib/Alectinib/Brigatinib/Lorlatinib/化疗/Atezolizumab;BRAFV600突变的病人,一线治疗可选Dabrafenib/trametinib;ROS1重排的病人,一线治疗可选Crizotinib。
8. 携带其他可驱动基因的治疗建议
针对RET/MET扩增/MET14外显子变异/HER2/NRTK融合等这些基因,建议入组相关的临床试验。
9. 放疗在晚期NSCLC的地位
放疗可对包括咯血、有症状气道阻塞、胸痛、骨转移、上腔静脉综合征及软组织/神经侵犯等起到缓解症状的作用;高剂量放疗不一定能最大程度缓解症状;体外放疗比支气管内近距离放疗更有效;对脊髓压迫进行早期放疗可有效缓解神经系统症状。
10. 脑转移及脑膜转移
WBRT的适用对象需基于病人的预后因素判断;单发脑转移可推荐SRS或者手术切除,且切除术后建议予WBRT或SRS;2-4个脑转移病灶可推荐SRS;SRS代替WBRT的情况下,放疗术后需行头颅MR做密切随访;驱动基因(EGFR/ALK)阳性、无症状脑转移的病人,推荐首选TKI而推迟放疗;免疫位点抑制剂对脑转移的疗效及安全性仍未明,暂不予推荐;脑脊液细胞学诊断脑膜转移具有低敏感度及高特异度;脑膜转移的病人可选择血脑屏障透过率较高的二代TKI;鞘内注射药物在某些情况下可以考虑用于脑膜转移的治疗。
11. 寡转移及骨转移的治疗
1-3个同步转移病灶的病人予以全身治疗和局部干预后,可获得较长的DFS,但方案的制定需由MDT讨论决定;具有少数异时转移病灶的病人可予高剂量放疗或手术做干预,干预后可获得较长DFS;携带驱动基因的病人使用TKI期间出现寡转移局部进展时,可予高剂量放疗或手术做干预,干预后可获得较长DFS;以上建议的证据支持来源于回顾性的数据,因此参加临床试验更予推荐;对侧肺出现单发转移的建议予以手术切除。唑来磷酸可降低骨转移相关并发症的发生,但地诺单抗可能由于唑来磷酸;在控制骨转移相关的疼痛时,单次放疗不亚于多次分割放疗。
12. 微创手术及姑息治疗
激光、冷冻疗法、支架放置可用于有症状气道阻塞或梗阻性感染的治疗;内镜可用于咯血的诊治;上腔静脉综合征采用血管内放置支架予以控制。早期可行姑息治疗,且与全身的抗肿瘤治疗同时进行。
13. 随访:
每6-12周一次随访,以保证二线治疗的尽早启用。
本次由亚洲肿瘤学专家们达成的共识已在线发表于Annals of Oncology,大部分指南都获得了专家们一致的同意。共识的提出不仅基于ESMO发布的在欧洲实行的指南,而且有足够的科学证据予以支持。但值得注意的是,该指南的建议未考虑某些药物在各个国家获批的情况,因此某些建议仍需按照国情进行选择性采纳。
泛亚ESMO指南发布后,广东省肺癌研究所的吴一龙教授表示:
“欧洲肿瘤学会委托CSCO和CTONG牵头组织的泛亚ESMO晚期非小细胞肺癌指南,在亚洲地区6大肿瘤学会的参与下,由中国学者领衔,历经1年多的锤炼,23项200多条细则终于取得共识。有意思的是,亚洲专家几乎一致的认为靶向药物必须有靶,因此对ESMO指南中特罗凯和阿法替尼一定情况下可用于没靶的肺癌投出了反对票;坚持了EGFR突变对药物选择的绝对性。需警示的是,中国的药物可及性远比不上亚洲其他国家和地区,中国任重道远啊!这部指南非常接地气,非常适应东亚地区使用。”

本次指南为东亚地区的临床医生提供了非常实用的参考,值得我们的学习。
参考文献:
Y -L Wu; D Planchard; S Lu; H Sun, et al. Pan-Asianadapted Clinical Practice Guidelines for the management of patients withmetastatic non-small-cell lung cancer: a CSCO–ESMO initiative endorsed by JSMO,KSMO, MOS, SSO and TOS. Annals of Oncology, Volume 30, Issue 2, 1 February2019, Pages 171–210, https://doi.org/10.1093/annonc/mdy554.
推荐阅读
文章评论
注册或登后即可发表评论
登录/注册
全部评论(0)